- 学科导航
丙肝治疗:直接抗病毒药物可行吗?
|
编者按 2013年,直接抗病毒药物(DAA)发展迅猛,已有多种DAA通过美国食品与药物管理局(FDA)批准上市,并被FDA指定为突破性疗法。该药物具有免于注射可以口服、持续病毒学应答(SVR)率高、疗程较短等优势,给丙型肝炎(丙肝)患者,特别是不能耐受干扰素(IFN)治疗的患者带来了希望。但目前DAA的成本居高不下,患者负担能力有限,限制了DAA的推广使用。有研究显示,IFN与利巴韦林(RBV)合用5年以上仍能保持较高的SVR,而DAA药物能否也具有同样的疗效,尚需进一步临床试验证实。魏来教授和高嘉宏教授将一同回顾DAA药物的研发历程,细数DAA药物的个中利弊,把握DAA今后发展的脉搏。
DAA药物,逐一细说
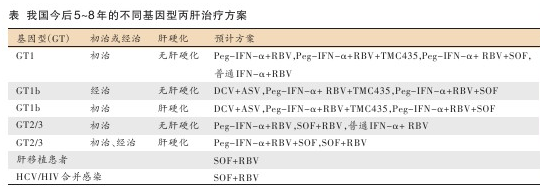
“由于我国的慢性丙肝患者IL-28B基因型有利于聚乙二醇干扰素α(Peg-IFN-α)联合RBV的应答,且DAA上市后的价格较高,故Peg-IFN-α联合RBV的方案仍有可能在我国维持一段时间,并随着国产Peg-IFN-α的上市而有更多的患者获益。在今后一段时间,对不同基因型患者,我们将有不同的治疗选择(表)。”
2013年丙肝抗病毒治疗的重要进展为simeprevir(TMC435)和sofosbuvir(SOF)获得FDA批准上市,daclatasvir(DCV)联合asunaprevir(ASV)在基因1b型感染者中SVR率达80%以上。
TMC435是靶向丙型肝炎病毒(HCV)蛋白酶的抑制剂。2013年11月美国FDA批准该药上市,该药是首个获批的每天口服1次的蛋白酶抑制剂。其安全性良好,无致突变性,不会引起染色体断裂。QUEST-2研究显示,TMC435联合Peg-IFN-α加RBV的SVR较未联合TMC435患者高。我国已在2012年10月启动该药的临床试验。
SOF是HCV非结构基因5B聚合酶的核苷(酸)类似物。2013年12月FDA批准该药上市,是首个获批的泛基因型直接抗HCV药物。该药服用疗程仅为12周,是首个用于肝移植、丙肝肝癌患者的抗病毒药物,也是首个用于HCV和人类免疫缺陷病毒(HIV)合并感染患者的直接抗HCV药物。我国已开始申请该药的临床试验。
DCV是靶向HCV非结构5A基因的抑制剂,ASV是蛋白酶抑制剂。日本基因1b型HCV感染者评价DCV联合ASV安全性和有效性的开放、平行Ⅲ期临床研究结果显示,治疗12周后,患者SVR为85.6%。
DCV临床试验已于2013年5月27日获得国家食品药品监督管理总局(CFDA)批准,6月20日在北京大学第三医院开始Ⅰ期临床研究。ASV临床试验于2013年6月20日获得CFDA批准,8月27日在上海徐汇区中心医院开始Ⅰ期临床研究,并将在2014年开展用于无法耐受或禁忌IFN-α治疗或IFN-α联合RBV治疗的基因1b型HCV感染受试者的Ⅲ期、非盲法研究。
DAA取代现有疗法尚需时日
“尽管全口服的DAA对患者是莫大的福音,也是应走的道路,但其价格昂贵,若纳入医疗保障体系,将对亚洲各国的医疗保险预算发生重大冲击。亚洲丙肝患者对现存相对便宜的IFN与RBV治疗已有不错的效果,如何适当使用DAA以增加疗效并减少医疗支出将是下一个研究热点。” 目前大多数亚洲国家对丙肝的标准治疗是注射长效型IFN(Peg-IFN)与口服RBV合用。采用应答指导治疗,该疗法对75%以上的HCV基因1型患者有效,对基因2型的患者效果更好,治愈率可达90%~95%。但据调查,仍有半数的丙肝患者因副作用严重而不愿接受Peg-IFN与RBV治疗。
HCV属易产生变异的正单股RNA病毒,有3个较重要的非结构区酵素酶和蛋白控制病毒复制:蛋白酶(NS3protease)、RNA聚合酶(NS5B polymerase)和NS5A蛋白。因此,开发DAA药物如蛋白酶、RNA聚合酶和NS5A蛋白抑制剂就成为研究方向。
2011年5月,FDA分别通过两个第1代口服蛋白酶抑制剂――telaprevir(Vertex)和boceprevir(MSD),但仍须同时使用IFN和RBV(简称3合1治疗),且患者副作用严重。3合1治疗患者退出比率从Peg-IFN和RBV联用时的10%提升至20%,肝硬化患者治疗退出率更高达40%。
此外,全口服无需联用RBV的2合1(DUAL)新处方(第2代蛋白酶抑制剂合用NS5A蛋白抑制剂)已在日本完成Ⅲ期临床试验,针对亚洲常见的基因1b型患者可不需合用IFN与RBV,该药有望明年在日本上市,将成为亚洲首个全口服的丙肝药物。
来源:中国医学论坛报 |

热门新闻
- 阅读
- 评论
推荐阅读
-
儿童感染后用什么药?哪些情况需要就医?北
儿童感染新冠病毒的症状、病程有何特点?退烧药怎么选、怎么吃?孩子出现何种症状需立[详细]
-
国务院最新公布:我国医养结合面临问题和下
导语医养结合将成为下一个风口!在日前召开的第十三届全国人大常委会第三十六次会议上[详细]
-
版权所有:北京英芙麦迪科技有限公司
地址:北京市顺义区竺园二街2号院8号楼301(天竺综合保税区)
电话:(010)-80489293-6011 邮件:hmp@bjhanmi.com.cn
-
 互联网药品信息服务资格证书 京ICP备07502511号-4
互联网药品信息服务资格证书 京ICP备07502511号-4药品医疗器械网络信息服务备案 (京)网药械信息备字(2022)第00010号
(京)-非经营性-2019-0001
 京公网安备11011302001972
京公网安备11011302001972

 收藏
收藏






